PEG-N3與炔基的生物正交和點擊化學
生物正交化學簡介
生物正交化學是指在不影響生物分子或幹擾生化過程的情況下,在生物環境中發生的一系列反應。爲達到此目的,反應必須滿足快速、高效和特異性的要求。
• pH值:反應必須在生理環境的溫度和pH值下發生;
• 精準:反應必須具有選擇性并且高效得到目标産品,且須不受水或内源性親核試劑、親電試劑、還原劑或複雜生物環境中氧化劑的影響;
• 快速:即便在低濃度下,反應也必須是快速的,并且須生成穩定的反應産物;
• 特異性:反應應涉及生物系統中非天然存在的官能團。
生物正交反應的優點和缺點
|
生物正交反應
|
優點
|
缺點
|
|
Staudinger
連接反應
|
疊氮化物和膦化物具有生物相容性,生成的産物是以穩定的酰胺鍵連接的。
|
反應速度慢,磷化氫容易被氧化。
|
|
CuAAC(疊氮+炔基)
|
反應迅速,在20 μM Cu(I)的催化下k值可達~10-100(M-1S-1);具有良好的區域選擇性。
|
盡管有些配體如THPTA比較穩定,但是銅催化劑的銅毒性仍需考慮在内。
|
|
SPAAC(疊氮+DBCO)
|
無需銅催化,k值約~1-60 (M-1S-1)。
|
1. 反應慢于CuAAC,大塊的環狀砌塊難以融入生物分子;
2. 所需溶劑:10%-40%的乙醇溶液或DMSO(至多60%)/PBS緩沖液;
3. pH < 5.5時反應速度會變慢,因爲在此pH下DBCO的穩定性會降低;
4. 巯基、疊氮化鈉都會與DBCO發生反應。
|
|
IEDDA (TCO + Tz)
|
反應非常迅速,k值約~1-106 (M-1S-1)
|
TCO在含水環境中穩定性差。
|
• CuAAC:銅催化的疊氮-炔基環加
• SPAAC:疊氮-烷烴環化加成反應
• IEDDA:逆電子需求的D-A反應。
表1:各類生物正交反應的優缺點小結表
疊氮-炔基點擊化學簡介
經典的點擊化學反應會用到銅作爲催化劑,一般是一價銅催化1,3-偶極環加成炔和疊氮化物形成1,2,3-三唑[1,2]。一價銅的來源包括碘化銅、溴化銅、
銅屑或硫酸銅與還原劑發生反應生成的産物[3]。然而,一價銅具有熱力學不穩定性,容易被氧化成無活性的二價銅,通常需要銅催化劑與合适的螯合配體共同制備。
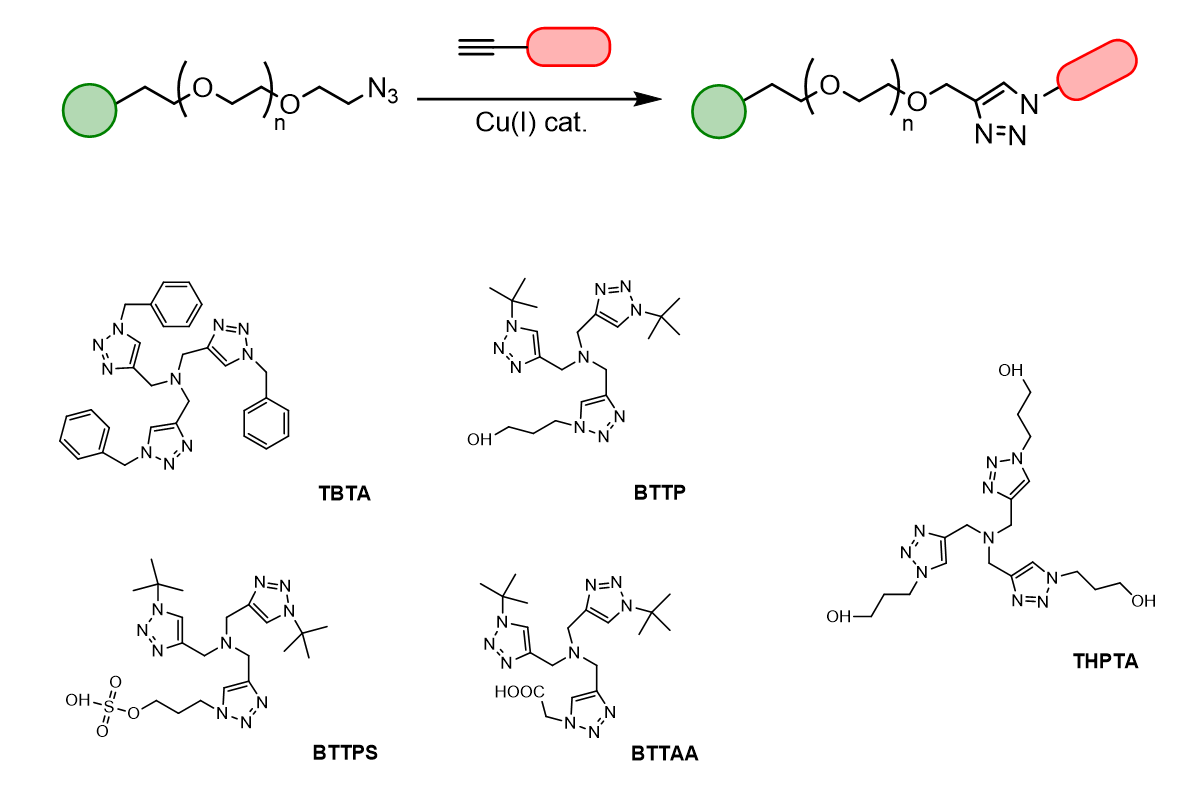
優化後的點擊化學反應是使用了用抗壞血酸鈉和一價銅穩定的配體三(苄基三唑基甲基)胺(TBTA)還原硫酸銅來原位制備一價銅Cu(I)。通過這個方法,可以避免溶解氧氧化催化一價銅,因此能夠使得點擊化學反應更爲有效。在典型的點擊化學中,硫酸銅是與TBTA預絡合的,現将這種複合催化劑與炔和疊氮化物混合,随後再加入抗壞血酸鈉來引發點擊反應。
TBTA覆蓋了在點擊化學領域的大量實際應用,除了含水環境下的共轭反應。而水溶性的THPTA點擊配體則可以适用于水相反應,進一步簡化點擊化學步驟,爲點擊化學反應提供具生物相容性的THPTA配體來結合Cu(I),阻斷Cu(I)的生物利用度,改善其潛在的毒性作用,保持催化效率
[4]。同時THPTA配體可以有效地被用于高效标記活細胞,并維持細胞活性[5]。
我們發現THPTA在水相反應中是一種高效的點擊化學配體,它的标記反應在室溫下往往隻需要15-30分鍾即可完成。在冷凍條件下儲存,配體CuSO4
複合物在至少一個月後仍能保持原有的活性。
實操案例
寡核苷酸類和DNA的标記
1. 配制以下原液:
• 200 mM THPTA配體的水溶液
• 100 mM硫酸銅水溶液
• 炔基标記的水相寡聚物
• 100 mM抗壞血酸鈉水溶液
• 10 mM在DMSO/叔丁醇或水中的含疊氮化合物
2. 在反應前将硫酸銅和THPTA配體以1:2的當量比混合靜置幾分鍾,這樣的溶液在冷凍後可以穩定儲存數周;
3. 向寡聚糖/DNA溶液中添加過量4~50倍當量的疊氮化物(如PEG-N3等);
4. 添加25當量的THPTA/CuSO4;
5. 添加40當量的抗壞血酸鈉;
6. 在室溫下靜置反應30~60分鍾;
7. 在乙醇中沉澱純化寡聚物。
細胞裂解物的标記
1. 配制以下原液:
• 100 mM THPTA配體的水溶液或緩沖溶液
• 20 mM硫酸銅水溶液
• 300 mM抗壞血酸鈉水溶液
• 2.5 mM在水或DMSO中的炔基或疊氮标記試劑
2. 對每個疊氮化物或炔基修飾的蛋白質裂解物樣品,添加以下物質至1.5 mL的離心管中,然後簡單渦旋混合:
• 50 µL存放于蛋白質萃取緩沖液中的蛋白質裂解産物(1-5 mg/mL)
• 90 µL PBS緩沖液
• 20 µL在水中或DMSO中2.5 mM相應疊氮化物(或含炔基化合物)的檢測試劑
3. 加入10 µL的100 mM THPTA溶液并簡單渦旋混合;
4. 加入10 µL的20 mM硫酸銅溶液并簡單渦旋混合;
5. 加入10 µL的300 mM 抗壞血酸鈉溶液來引發點擊化學反應并簡單渦旋混合;
6. 保護反應避光,并在室溫下反應30分鍾;
7. 現在在裂解物中的蛋白質已通過點擊化學反應被标記了,可以進行下一步的處理和分析了。
銅催化的炔基-疊氮化物點擊化學标記活細胞
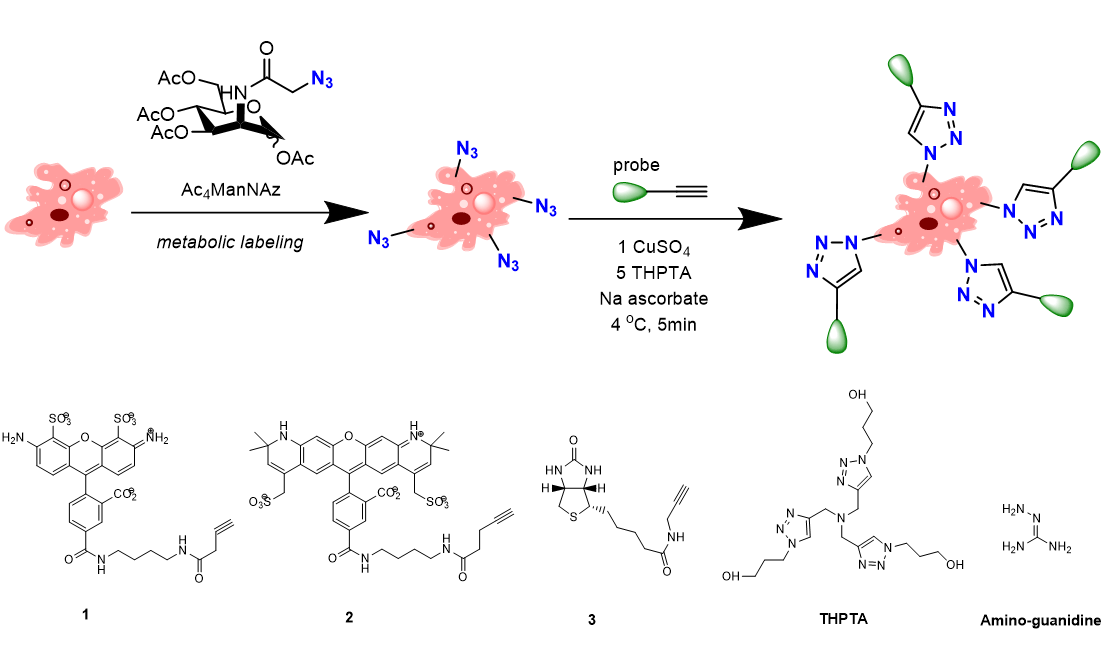
圖1:(上圖)細胞标記的步驟
(下圖)炔基探針試劑和催化劑添加劑
疊氮聚糖在HeLa和CHO細胞表面的标記及共聚焦顯微鏡成像
将細胞以1 × 105個/mL的濃度置于35 mm玻璃底培養皿中培育,并在含有或不含50 μM Ac4ManNAz的生長培養基(含10%胎牛血清、1%谷氨酰胺和1%青鏈黴素溶液的MEM培養基)中在37 ℃和5% CO2的條件下過夜反應。輕輕地抽吸培養基将多餘的溶液移除,用1 mL DPBS洗滌細胞2次。在微量離心管中,4 ℃下以1:5的摩爾當量比将硫酸銅和THPTA添加到含有染料-1炔基或2炔基(濃度:25 μM)的DPBS和氨基胍(濃度:1 mM)中。配制新鮮制備的抗壞血酸鈉原液(100 mM)便于後續配制最終濃度爲2.5 mM的抗壞血酸鈉溶液。将該反應混合物在4 ℃條件下冰浴保溫10分鍾,然後添加到細胞中。将此混合物再次在4 ℃保溫5分鍾之後,洗滌細胞,室溫下用3%多聚甲醛、0.3%戊二醛和1 mM的氯化鎂混合溶液在DBPS中固定10分鍾。加入4', 6-二脒基-2-苯基吲哚(DAPI)對細胞核進行染色,并在每一步之間,用DPBS沖洗玻片3次,玻片采用Vecta Shield介質來安裝;使用Bio-Rad 2100共聚焦顯微鏡和60×的油鏡來進行切片成像,用ImageJ(http://rsbweb.nih.gov/ij/)來分析和處理得到的數據及圖片。對于雙标記的實驗,在标記反應後,用1 mL的生長培養基洗滌細胞兩次,然後重新置于含有50 μM的Ac4ManNAz的培養基放置繼續培育20 小時。細胞表面标記的最佳條件爲在4 ℃的培養基中,用25 μM的炔基化合物溶液、硫酸銅溶液(50 μM)、THPTA (250 μM)、氨基胍(1 mM)和抗壞血酸鈉(2.5 mM)标記1-5分鍾。
參考文獻
1. Polytriazoles as Copper(I)-Stabilizing Ligands in Catalysis; T. R. Chan, R. Hilgraf, K. B. Sharpless, V. V. Fokin, Org. Lett. 2004, 6, 2858. https://pubs.acs.org/doi/10.1021/ol0493094
2. Analysis and Optimization of Copper-Catalyzed Azide–Alkyne Cycloaddition for Bioconjugation; V. Hong, S. I. Presolski, C. Ma, M. G. Finn, Angew. Chem. Int. Ed. 2009, 48, 9879. https://onlinelibrary.wiley.com/doi/10.1002/ange.200905087
3. Stabilization of Virus-like Particles with Poly(2-oxazoline)s; F. Manzenrieder, R. Luxenhofer, M. Retzlaff, R. Jordan, M. G. Finn, Angew. Chem. Int. Ed. 2011, 50, 2601. https://onlinelibrary.wiley.com/doi/10.1002/ange.201006134
4. Synthesis of Cyclic Peptide Disulfide–PHPMA Conjugates via Sequential Active Ester Aminolysis and CuAAC Coupling; K. A. Günay, H. Klok, Polym. Chem. 2016, 7, 970. https://pubs.rsc.org/en/content/articlelanding/2016/py/c5py01817j
5. Cellular Consequences of Copper Complexes used to Catalyze Bioorthogonal Click Reactions; D. C. Kennedy, C. S. McKay, M. C. B. Legault, D. C. Danielson, J. A. Blake, A. F. Pegoraro, A. Stolow, Z. Mester, J. P. Pezacki, J. Am. Chem. Soc. 2011, 133, 17993. https://pubs.acs.org/doi/10.1021/ja2083027
這有幫助嗎? 是 否 第一個投票!
标簽:
聚乙二醇(PEG) 生物正交化學 疊氮炔烴點擊化學 材料科學 生物醫學材料
相關産品列表
-
B122224 (+)-生物素-PEG2-疊氮化物 ,98%SDS| 價格
-
A163304 Azido PEG NHS, N3-PEG-NHS ,MW 5000 DaSDS| 價格
-
A163308 疊氮 PEG 巯基, N3-PEG-SH ,MW 3400 DaSDS| 價格
-
A163279 疊氮-PEG-胺,N3-PEG-NH2 ,95%,MW 10000 DaSDS| 價格
-
A163292 Azido PEG hydroxyl, N3-PEG-OH ,MW 2000 DaSDS| 價格
-
A163313 Azido PEG, mPEG-N3 ,95%,MW 2000 DaSDS| 價格
-
A163314 Azido PEG, mPEG-N3 ,95%,MW 20000 DaSDS| 價格
-
A163317 疊氮 PEG, mPEG-N3 ,MW 40000 DaSDS| 價格
-
A163316 疊氮 PEG, mPEG-N3 ,MW 350 DaSDS| 價格
-
A163315 疊氮 PEG, mPEG-N3 ,MW 30000 DaSDS| 價格
-
A163312 Azido PEG, mPEG-N3 ,95%,MW 10000 DaSDS| 價格
-
A163311 Azido PEG, mPEG-N3 ,95%, MW 1000 DaSDS| 價格
-
A166185 疊氮基PEG12-酸 ,95%SDS| 價格
-
A305020 疊氮-PEG4-NHS酯 ,95%SDS| 價格
-
B171421 Biotin PEG3 azide ,95%SDS| 價格
-
B122225 生物素-PEG3-疊氮化物 ,95%SDS| 價格
-
B152153 生物素-PEG₄-疊氮 ,>96.0%(HPLC)SDS| 價格
-
H163764 HO-PEG4-Azide ,95%SDS| 價格
-
S164289 矽烷-PEG-N3, 矽烷 PEG 疊氮 ,MW 5000 DaSDS| 價格

 訂購客服熱線
訂購客服熱線







 營業執照(三證合一)
營業執照(三證合一)  危險品化學品經營許可證(不帶存儲)
危險品化學品經營許可證(不帶存儲) 